
~特に安全性が求められる医療分野への応用に期待~
Genome editing
サマリー
- 従来法に比べ、オフターゲット(意図しない遺伝子の変異)が生じるリスクを10分の1~100分の1に低減。2種類の変異(ピンポイントの変異と長い欠失)を導入可能。
- 海外知財のライセンスの使用を回避し、日本の大学発の公益性に配慮した技術。
- 医療分野をはじめ幅広いバイオ産業への応用が可能。
既存のゲノム編集技術における2つの課題――「オフターゲット」と知財
ゲノム編集とは、生物がもつゲノムDNAの狙った部位を切断し、その切断が修復される機構を介して、遺伝情報を書き換える技術です。あらゆる生物種の遺伝情報を狙った通りに改変できれば、新たな治療技術の創出や医薬品開発、農畜水産物の品種改良などに繋がるため、さまざまな分野への応用が期待されています。
現在は、「CRISPR-Cas9(クリスパー・キャスナイン)」というゲノム編集技術が、簡便さと編集効率の高さから世界的に広く利用されています。この技術は、DNAの標的配列を認識するガイドRNAと、認識した部位を切断するCas9というタンパク質が細胞内で共に働くことでDNAを改変することができます。ダウドナ博士とシャルパンティエ博士が共同で開発し、2020年にノーベル化学賞を受賞しました。様々な生物で用いることができる画期的な遺伝子改変技術ですが、一方で、意図しない部位に変異を起こす「オフターゲット」が生じることがあり、特に安全性が求められる医療分野への応用においては課題となっています。
また、CRISPR-Cas9の知的財産権は海外にあり、商業利用の場合には高額なライセンス料が必要となります。CRISPR-Cas9以外にも様々なゲノム編集技術が使われていますが、そのほとんどは欧米で開発されたものであり、日本での実用化にあたっては日本発の知財があることが重要です。こうした状況を受け、「なんとか日本独自のゲノム編集ツールを開発したい」という思いから、刑部教授らは2016年にゲノム編集技術の開発に着手しました
オフターゲットのリスクを大幅に軽減した新技術「TiD」
CRISPR-Casシステムは、もともと細菌などがもつ免疫機構として発見されたもので、自然界にはCas9以外にもさまざまなタイプのCRISPR-Casが存在します。刑部教授はそれらのうち、これまで機能が不明であったCRISPR-CasタイプⅠ-Dに着目し、研究を重ねた結果、ゲノム編集に利用できることを見いだしました。そして、このシステムを「TiD」と名付け、2020年に植物の細胞で、2021年にヒト細胞でゲノム編集ができることを報告しました。
「TiDシステムは狙った配列を高精度に認識する特異性の高さが最大の特徴です。CRISPR-Cas9と比較して、オフターゲットが生じるリスクを10分の1~100分の1に抑えることができます」と刑部教授はいいます。一般にゲノム編集でオフターゲットが生じるのは、ゲノム上に標的配列と似た配列があると、そこにガイドRNAが結合してしまうためです。「CRISPR-Cas9では標的とするDNA配列が20塩基と短いので、ゲノム上に似たような配列がたくさんありますが、TiDシステムでは35~36塩基の配列を標的とします。単純なことですが、標的配列が15~16塩基長くなるだけで、ゲノム上の似ている配列の数が大幅に減り、オフターゲットが生じにくくなるのです」(刑部教授)。
2種類の変異を導入できる
特異性の高さだけでなく、導入できる変異の様式が2種類あることもTiDの特徴です。解析結果から、TiDはCRISPR-Cas9と同様にピンポイントの変異(数塩基程度の短い挿入または欠失など)をゲノムに導入できるのに加え、15kbp(15000塩基対)以上にも及ぶ、遺伝子領域全体を欠損するような長い欠失を導入できることもわかりました(図)。TiDではCas10dと呼ぶタンパク質がDNA切断活性をもっており、変異導入に重要な役割を果たしています。既存のゲノム編集ツールにはない特徴をもつことから、海外の知財に抵触しない新しい技術としてすでに特許を取得しています。
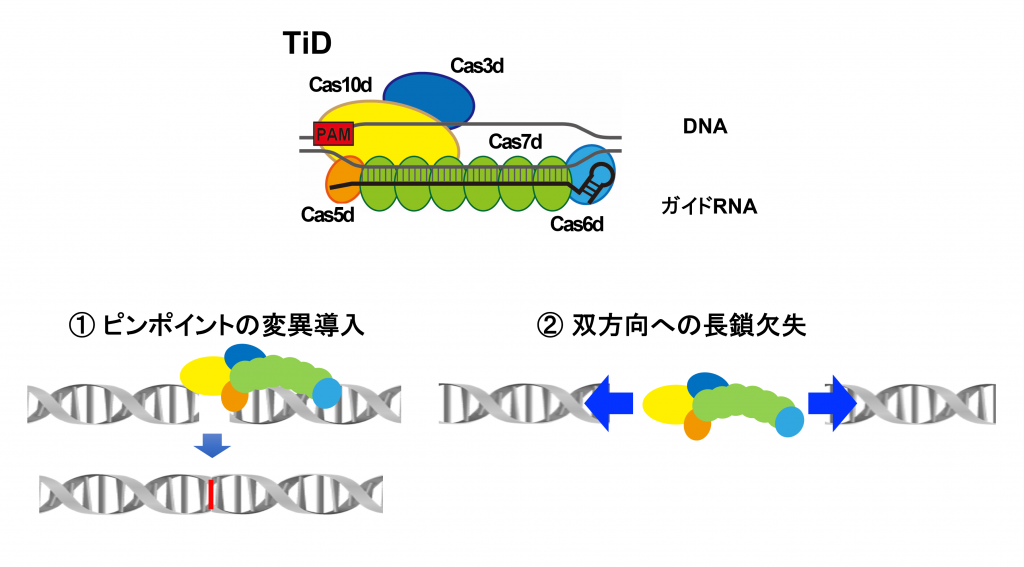
TiDは複数のタンパク質からなる複合体である。既存のCRISPR-Cas9と同様に、TiDはガイドRNAと相補する標的DNAを認識して結合しDNAを切断するが、標的配列長は35~36塩基、DNA切断に重要なタンパク質はCas10dであるという特徴をもっている。切断後に導入される変異には、①標的箇所における短い塩基配列の挿入または欠失(ピンポイントの変異導入)などと、②双方向への長い塩基配列の欠失の2つの様式がある。
一方で、課題もあると刑部教授はいいます。「TiDシステムでは複数のタンパク質が複合体を形成してゲノム編集が行われます。そのため、複数のタンパク質を同時に細胞内で発現させて機能させる必要があり、課題となっていました。現在までに、技術改良を重ねることで、使い勝手や効率がかなり向上した技術として使用が可能となってきました。さらなる向上を目指すとともに、さまざまな生物種でTiDによる遺伝子改変の応用例を示し、産業応用へつなげたいと考えています」
企業との連携、その先の展開
TiDの開発をはじめ刑部教授が行ってきた植物の基礎研究や技術開発は世界的に高く評価されており、クラリベイト社が発表する高被引用論文著者(各研究分野において被引用数が上位1%の論文の著者から選ばれる)に、刑部教授は2016~2022年の間に計6回選出されています。
TiDに対する産業界からの注目度も高まっており、すでに企業との連携も進めています。「TiDはオフターゲットのリスクが低いので、細胞治療や遺伝子治療、創薬など医療分野で特に有益なツールになります。そのほか、農業や畜産における品種改良や、生物を利用した物質生産など、活用できる分野は多岐にわたります。ゲノム編集の利用をこれから検討しようという企業の研究者の方からのご相談もお受けします。実際にどのように利用なさりたいのかを、研究者の方から具体的にうかがうことが、私たちもさらによい技術をつくるきっかけになると思っています。TiDを手軽に使えるようなキットの提供など、事業化も検討しているところです」。
刑部教授らの国産技術により、今後、日本の産業界・学術界でゲノム編集を用いた研究開発が活発になると期待されるなか、「未来を担う若い人たちが目を輝かせて研究に携わりたいと思えるような魅力ある研究基盤を、企業をはじめいろいろな立場の方たちとつくっていきたい」と刑部教授は意欲を見せています。
参考リンク
Flintbox
Novel genome engineering technology
https://oip-titech.flintbox.com/technologies/bdfdc769-681e-4c6b-9354-5db29852d50a
東工大生命理工学系 News【研究室紹介】刑部研究室
https://educ.titech.ac.jp/bio/news/2021_10/061375.html
NEDOニュースリリース
世界初、新規ゲノム編集技術「TiD」で植物の遺伝子改変の有効性を実証
―日本のバイオインダストリー推進の原動力として期待―
https://www.nedo.go.jp/news/press/AA5_101384.html
東工大ニュース「刑部祐里子教授が2022年版クラリベイト社の高被引用論文著者に選出」
https://www.titech.ac.jp/news/2022/065497
GTIE2022 GAPファンド 「新規国産ゲノム編集TiDの基盤技術開発」
https://gtie.jp/gap-fund/39651/



